Gustavo Covelli, paciente Gaucher, conoció su enfermedad a la edad de 30 años cuando no se tenía mucha información sobre la misma.
“A esa edad uno es el dueño del mundo, se siente invulnerable y conocer un diagnóstico de este tipo es frustrante, pues uno no ve un horizonte claro de su salud. También significa una aceptación de que la vida va a deteriorarse y eso no es nada fácil”, así recordó Gustavo lo que sintió ese día de 1981, cuando su doctor le dijo que tenía la enfermedad de Gaucher.
Esta enfermedad poco usual tiene un día al año para ser conmemorada, con el fin de crear conciencia y visibilizar a quienes la padecen. La fecha estipulada, desde el 2014, es el 1 de octubre.
¿Qué es?
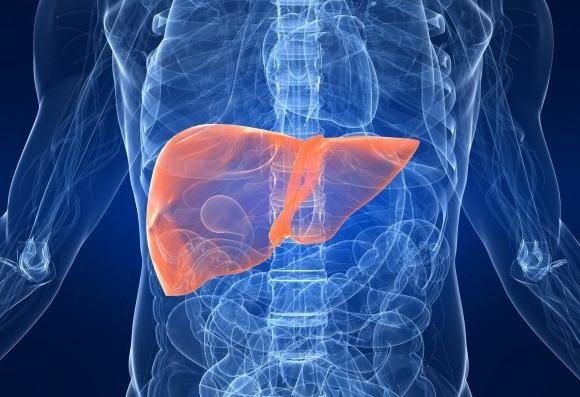
El doctor Jheremy Reyes, especialista en medicina interna y hematología de la Clínica Los Nogales, explicó que “Gaucher es una enfermedad huérfana, es decir, poco frecuente, que se caracteriza por la alteración genética de una enzima denominada glucocerebrosidasa (GBA), la cual destruye al glucocerebrósido que, al acumularse en varias zonas del cuerpo, daña tejidos y órganos, especialmente el bazo, el hígado, la médula ósea y los huesos”.
En pocas palabras, es cuando el organismo produce de forma deficiente la enzima que se encarga de descomponer al glucocerebrósido, un tipo de lípido que, al almacenarse, afecta el normal funcionamiento de la médula ósea, el bazo, el hígado y puede llegar, incluso, a destruir los huesos.
Además, se trata de una patología congénita y genética cuyos síntomas pueden manifestarse en la infancia, la juventud o en la vida adulta.
El problema es que como esta enfermedad no es frecuente en la población, los médicos poco piensan en ella, entonces puede pasar mucho tiempo para diagnosticarla
Gustavo fue asintomático hasta 1979, cuando asistió al médico por fuertes dolores en la cadera. Tras varios estudios se descubrió que el hueso estaba desgastado y, aunque era un procedimiento inusual para su edad, lo operaron.
“Después aparecieron los otros síntomas; problemas hepáticos y otra serie de problemas hematológicos. Ahí comenzó la incertidumbre y las preguntas, ‘¿esto por qué?’, ‘¿esto qué es?’. Entonces, es un momento que es frustrante en el sentido de que se siente uno enfermo, está enfermo, recluido en un hospital y no sabe qué es”, relató el hombre.
“El problema es que como esta enfermedad no es frecuente en la población, los médicos poco piensan en ella, entonces puede pasar mucho tiempo para diagnosticarla, pero en la actualidad, si tú piensas en la enfermedad, el diagnóstico es relativamente sencillo”, aseguró el doctor Reyes.
Al no producirse la enzima Glucocerebrosidasa los lípidos que ésta debería eliminar se acumulan afectando el hígado, el bazo y los huesos.
En el caso de Gustavo, ningún médico comprendía lo que pasaba, así que fueron momentos de angustia, dudas y temores. Las horas parecían andar a paso lento, mientras los días se le pasaban en la cama de un hospital entre exámenes médicos y encuentros con especialistas.
El diagnóstico
“Después de muchos exámenes se logró el diagnóstico en el año 1981. Lo hizo un médico investigador universitario. Me dijo: ‘Esta es una cuestión muy rara, realmente es algo que lo tienen muy pocas personas’” recordó.
Además, señaló que para la época sólo en los libros de medicina interna se encontraba información sobre el tema, pero “nada específico, y no había tratamientos, sino simplemente paliar la enfermedad y manejar los síntomas”.
Esa era la peor parte: el saber que nada podía hacer para cambiar lo que le estaba pasando.
“Cuando te dicen el diagnóstico, pues bueno, es un descanso, pero cuando uno comienza a mirar sobre la enfermedad uno se siente muy solo, porque es una enfermedad muy rara. La información que se consigue es poca y lo que dice el médico es que tengo que vivir con ella porque no hay nada que hacer”, relató Gustavo.
Pasan los años, avanza la enfermedad
Gustavo aceptó su diagnóstico e hizo lo posible por mantener una vida normal. Años más adelante, en 1984, conoció a Luz Victoria Salazar con quien se casó en 1988. Tuvieron dos hijos y continúo con sus días como de costumbre.
Pero con el tiempo los síntomas se agudizaron y afectaron el desarrollo de sus actividades.
Luz Victoria ha acompañado a Gustavo desde hace más de 32 años.
“El problema hematológico en el día a día se traduce en cansancio crónico. Yo en ese momento estaba trabajando y era productivo, pero tenía que hacer un esfuerzo muy grande para mantenerme competitivo. El problema en la sangre me hacía sentir supremamente débil e incapaz de hacer las cosas”.
En 1993, el avance de la enfermedad llegó al punto de amenazar su vida.
“Mi médica me dijo: ‘Gustavo, esto pronto desembocará en una cirrosis y van a generarse unos problemas grandes, es mejor que vaya organizando su vida’. Esa fue una situación muy difícil. Pienso que la parte más difícil de la enfermedad es cuando tú sabes que el tiempo está contado”, aseguró.
Eso es durísimo… Uno no está preparado para que le digan el pronóstico de vida
Luz Victoria
Si bien es cierto que es el paciente quien sufre los dolores de la enfermedad, los cuidadores también reciben toda una carga emocional y, a veces, física que los desgasta. En el caso de Luz Victoria, aunque su esposo nunca dependió de ella, sí tuvo que resistir al sinsabor de un futuro incierto y la impotencia de no saber cómo ayudar a su ser amado.
“Llegando al momento en que el diagnóstico era tan malo, tan preocupante, realmente hubo mucha angustia”, contó Luz, al tiempo que agregó que de esos obstáculos nacieron las “ganas de luchar por encontrar la forma de cambiar el rumbo de la historia”.
Una esperanza
“Salí a almorzar con un amigo y pasó un médico que conocía mi condición. Nos saludamos y me dijo: ‘Oye, Gustavo, me acordé de ti porque hay un tratamiento para tu enfermedad’.
Así recordó Gustavo esa tarde de 1994, cuando la vida lo sorprendió con una luz de esperanza.
El profesional había leído en una revista que un laboratorio, en EE.UU., había desarrollado el tratamiento para la enfermedad de Gaucher.
“Busqué la revista en su consultorio. ¡Eso fue increíble! Fotocopié las hojas y me fui a donde mi doctora tratante”, relató Gustavo.
El primer paciente tratado en Colombia
La doctora que atendía a Gustavo le confirmó que había un medicamento. Semanas antes había viajado a un congreso en México, donde le entregaron toda la información.
Se contactaron con el laboratorio, que también se interesó por el caso, e iniciaron la lucha por encontrar la forma de que el fármaco llegara al país. Pero no fue nada fácil. En ese momento Colombia estaba en plena transición a la Ley 100.
Encontrar una luz después de esa desesperanza realmente fue súper importante para nosotros. Y tratar de conseguir el tratamiento fue una labor, de verdad, titánica.
Luz y Gustavo pasaron meses de oficina en oficina, pero nadie se apropió de su caso. Cansados de que ninguna entidad les respondiera, decidieron acudir a la acción de tutela.
“Fue un momento muy grande en nuestras vidas, era un triunfo después de un año y medio de lucha. Llegar a un fallo de tutela que amparara ese derecho fue un momento de inmensa felicidad”, expresó Luz.
Gustavo estuvo muy involucrado en la importación del medicamento y, finalmente, en junio de 1996, tras una serie de estudios y protocolos, tuvo su primer tratamiento de remplazo enzimático.
Una nueva vida
Desde entonces han pasado 25 años. Gustavo pudo ver crecer a sus hijos y, aunque es una enfermedad que lo acompañará para siempre, aprendió a vivir con ella sin negarse a la posibilidad de llevar una vida normal.
“Las dificultades que se generaron con la cadera no se podían reversar, pero muchos síntomas de la parte hepática, hematológica y del bazo mejoraron (…) He tenido la aplicación del tratamiento hace 25 años y el resultado ha sido muy bueno. Aquello que fue una situación oscura y difícil, se ha superado”, concluyó.
De hecho, en la actualidad, su esposa dirige la Asociación Colombiana de Pacientes con Enfermedades de Depósito Lisosomal (Acopel), en la que han trabajado, desde 1997, para ayudar a que otras familias encuentren el apoyo y la asesoría que requieren sobre este tipo de diagnósticos.
Tan pronto se enteraron de la existencia de un tratamiento para la enfermedad de Gaucher la pareja inició su lucha para que el medicamento llegara al país.
Lo anterior, teniendo en cuenta que, como Gustavo, hay más de 52.000 colombianos que padecen alguna de las 2.198 enfermedades huérfanas registradas por el Ministerio de Salud. De ellas, Bogotá concentra alrededor del 19% de los casos, según cifras del Observatorio Interinstitucional de Enfermedades Huérfanas (Enhu).
El registro de estas enfermedades existe gracias a la Ley 1392 de 2010, la cual reconoce a las enfermedades huérfanas como condiciones de especial interés y estipula que el Estado colombiano debe garantizar la protección y cuidado de quienes las padecen.
De acuerdo con Luz Victoria, esta Ley ha jugado un papel importante en la visibilización de estas patologías, pero la lucha continúa, pues “se debe seguir trabajando en los aspectos sociales de la Ley, como la inclusión de los pacientes y el cuidado de los cuidadores”.
La idea es que todas las familias, como ocurrió con Gustavo, tengan acceso a sus tratamientos, pero, especialmente, a una mejor calidad de vida.
JESSIKA D. BONILLA BRAN
Tendencias EL TIEMPO
Fotos: Familia Gustavo Covelli
Imagen: iStock
Fuente: https://www.eltiempo.com/cultura/gente/enfermedad-de-gaucher-historia-del-primer-paciente-que-recibio-tratamiento-en-colombia-540857